A kannabinodok által okozta autofágia felhasználása melanóma sejtek elpusztítására
Journal of Investigative Dermatology
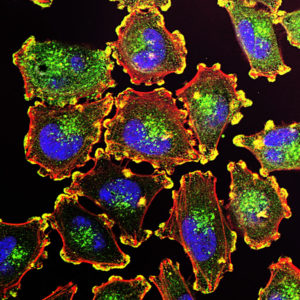
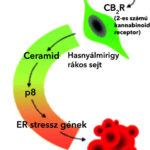
Bár a bőr melanóma előfordulás világszerte növekszik, az áttétes betegek túlélési aránya 10% alatt marad. Sürgősen új kezelési stratégiákra van szükség, különösen a BRAF/NRAS vad típusú tumorokat hordozó betegeknél. Az autofágia célzása a rákos sejtek halálának elősegítésére szolgál a kemoterápia-rezisztens daganatokban, és ennek a vizsgálatnak az a célja, hogy megvizsgálja azt a hipotézist, miszerint a kannabinoidok elősegítik az autofágia-függő apoptózist melanomában. A Δ(9)-tetrahidrokannabinollal (THC) végzett kezelés az autofágia aktiválódását, a sejtek életképességének csökkentését és az apoptózis aktiválódását eredményezte, miközben a klorokinnal való kezelés vagy az Atg7, de nem a Beclin-1 vagy Ambra1 csökkentése a kezelést megelőzően, megakadályozta a THC-indukálta autofágiát és sejthalát in vitro. A BRAF vad típusú melanoma xenograftokat hordozó egereknek a Sativex-szerű (egyforma mennyiségű THC-t és CBD-t tartalmazó laboratóriumi készítmény) beadása lényegében gátolta a melanoma életképességét, proliferációját és tumor növekedését, valamint ezzel páhozamosan megnövelte az autofágiát és az apoptózist, összehasonlítva a standard, egyetlen-szert-tartalmazó temozolomiddal. Összefoglalva, megállapításaink arra utalnak, hogy a THC aktiválja a nemkanonikus autofágia-mediált apoptózist a melanoma sejtekben, ami arra utal, hogy a Sativex-szel kiváltott citotoxikus autofágia klinikai értékelése szükséges metasztatikus betegség esetén.

A Δ9-tetrahidrokanabinol (THC) és a Sativex-szerű kannabinoidok elősegítik az autofágiát és a daganatellenes válaszokat melanoma xenograftokban.
A tumorszelektív sejthalált úgy érhetjük el, hogy a rákos sejtekben differenciálisan szabályozott útvonalakat célozzuk meg a normál sejtekhez képest. Ebben a vonatkozásban kimutattuk, hogy a normális emberi melanociták ellenállnak a THC-nak olyan koncentrációkban, amelyek melanomasejtekben sejthalált okoznak. Ez összhangban van azokkal a vizsgálatokkal, amelyek azt mutatják, hogy a rákos sejtek érzékenyebbek a THC-re és más kannabinoid receptor ligandokra a nem transzformált megfeleőikhez képest, a funkcionális CB-receptorok jelenléte ellenére (Velasco és munkatársai, 2012). A kannabinoidreceptorok szintetikus ligandumának melanomára kifejtett hatására utaló korábbi tanulmányokkal együtt (Blazquez és mtsai, 2006) ezek az adatok támogatják a kannabinoidok klinikai értékelését a fejlett stádiumú betegségben. Ezenkívül a THC aktiválja az autofágiát és az apoptózist mind a BRAF vad típusú, mind a mutált melanoma sejtvonalakban, ami arra utal, hogy az autofágia dereguláció (Armstrong et al., 2011; Corazzari et al., 2013) ellenére a THC valószínűleg hatásos melanómás tumorokban, függetlenül a BRAF mutációs állapottól. Továbbá megállapításaink azt mutatják, hogy a THC képes a melanoma sejtek életképességének és a tumor xenograft növekedésének történő csökkentésére önmagában, de ha alacsonyabb THC-dózist kombinálunk a CBD-vel, akkor az antitumor hatás fokozódik in vitro és legalább ugyanolyan hatásos volt, ami a THC önmagában in vivo. Ezenkívül a CBD apoptózist indukál reaktív oxigéngyökök előállításával és kaszpáz aktiváción keresztül a rákos sejtekben (Massi és mtsai, Shrivastava és munkatársai, 2011), jelezve, hogy a THC és a CBD különböző molekuláris mechanizmusokon keresztül együttműködnek a tumorsejtek halálának elősegítésében
(Shrivastava et al., 2011; Torres et al., 2011).