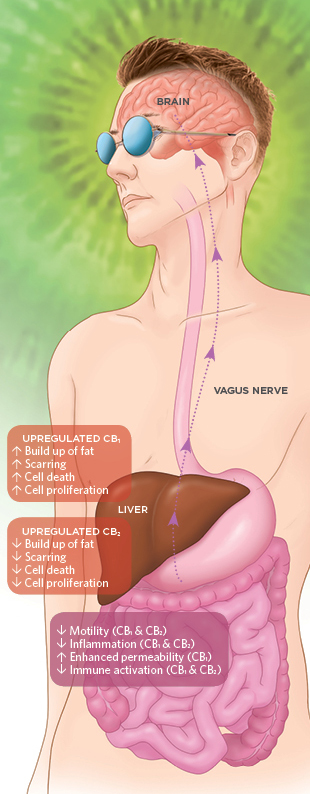
Az emberi szervezet tele van kannabisz-receptorokkal
Ugyanaz az endokannabinoid rendszer, amely miatt a kannabisz fogyasztásakor szervezetbe kerülő összetevők (fitokannabinoidok), pszichotikus állapotot alakítanak ki, fontos szerepet játszik az egészség megőrzésében és egyes betegséget kialakulásában az agyterületeken kívül is.
Nick DiPatriziot, neurofarmakológust zavarba ejtette ez a tény. Témavezetője a Californiai Egyetem kutatója, Daniele Piomelli 8 évvel korábban felfedezte, hogy az éhes patkányok szervezetében magasabb szinten vannak jelen az endokannabinoidok, azok az endogén molekulák, amelyek ugyanazokhoz a receptorokhoz kötődnek, mint a kannabisz növény aktív komponensei.
2009-ben, DiPatrizio kísérletet tett arra, hogy pontosan meghatározza, hogy ezek a molekulák hol és miként szabályozzák a táplálék felvételét patkányokban. A speciális diéta ellenére nem tudott meghatározni semmilyen eltérést az agyban, az endokannabinoidok tekintetében, annak ellenére, hogy az agy bővelkedik endokannabinoid receptorokban és nyilvánvalóan az a hely, ahol a viselkedéssel kapcsolatos jeleket keresni érdemes.
Piomelli óvaintette gyakornokát. „Azt mondta, ’Kezdesz neurocentrikussá válni. Emlékezz, hogy egy test is kapcsolódik a fejhez. Vizsgáld meg a test többi szervét is,” emlékszik vissza DiPatrizio. A fiatal kutató ehhez tartva magát végül felfedezte, hogy az éhség – és az elhízás – megnövekedett endokannabinoid szinteket eredményezett a jejunumban (éhbél), a vékonybél egy szakaszán. Az endokannabinoid rendszer a bélben, és nem az agyban szabályozza a táplálék felvételét rágcsálók esetében, mikor azok megízlelték a zsíros táplálékot.1
Az endokannabinoid rendszer kutatásának fejlődése tükrözi DiPatrizio korai gondolatait. Az 1980-as évek vége óta, mikor az első endokannabinoid receptort azonosították, a kutatók leginkább a központi idegrendszer vizsgálatára fókuszáltak. A fő kannabinoid receptort, a CB1-et, amely először patkány agyból került kimutatásra, napjainkban a leggyakoribb G-protein kapcsolt receptorként tartják számon a neuronokban. Mindemellett a kannabisz jól ismert pszichotróp hatásairól is. „Ezzel a kutatások nagyrészt központi idegrendszer-orientáltságúvá váltak” állítja Saoirse O’ Sullivan, aki a Nottingham Egyetemen (UK) tanulmányozza az endokannabinoidokat.
Egy ideje már tudjuk, hogy az agy képes szabályozni a bélműködést. Viszont úgy tűnik, hogy az endokannabid rendszeren keresztül a bélrendszer is képes módosítani az agy működését.
Újabb kutatások bizonyították, hogy az endokannabinoid rendszer – amely az endogén ligandokat, receptorokat és enzimet foglalja magában – nem csak és kizárólag az agyban van jelen. Test szerte mindenhol előfordul; szív, máj hasnyálmirigy, reproduktív szervek, stb. „Továbbra is sok ismeretlen része van ennek a rendszernek. Úgy tűnik, hogy minden fiziológiai működést szabályoz a szervezetben” – állítja DiPatrizio.
Jelenleg DiPatrizio egyetemi adjunktusként a Californiai Riversideban az Orvosi Egyetemen a teljes kutatási programját a bélrendszernek szenteli, ahol az endokannabinoid tűnik a normál és kóros működésének kialakulásáért felelős fő tényezőnek. A laboratóriuma feltételezése alapján az endokannabinoid szignalizáció (a bélrendszerben) vezet a nyugati típusú diéták túlevéses karakterisztikájához. Rágcsáló modellben a magas zsír és cukor tartalmú diéta krónikus túlfogyasztása a vér és bélrendszer megemelkedett endokannabinoid szintjéhez vezetett, további zsíros ételek bevitelére ösztönözve az állatot. Az endokannabinoidok receptorokkal való kölcsönhatását meggátolva azt tapasztalták, hogy csökkent a túlevés jelensége ezen állatok körében.2
Az étvággyal való kapcsolat arra ösztönözte a gyógyszercégeket, hogy az endokannabinoid rendszert célozzák meg annak érdekében, hogy kifejleszthessenek egy olyan fogyókúrás tablettát, ami csökkenti az étvágyat és kezeli az anyagcserezavart. Ezek az erőfeszítések napjainkban két tragikus kimenetelű és ismert hiba miatt a háttérbe szorultak. Azonban néhány kutató még mindig reménykedik abban, hogy egyszer sikerül megérteni ennek a rendszernek az igazi természetét és ez által képesek lesznek új terápiás eljárásokat kifejleszteni, legfőképpen a bélrendszer és az anyagcseréhez kapcsoltan.
„Elérkeztünk ahhoz a ponthoz, amikor is meg kell értenünk, hogy az endokannabinoidok hogyan lehetnek ilyen széles körben relevánsak – történetesen a szervezet minden egyes részén – állítja Mauro Maccarrone, a római Campus Bio-Medico Egyetem professzora, a biokémiai és molekuláris biológiai intézet vezetője, aki 1995 óta tanulmányozza ezeket a molekulákat. „Kell, hogy legyen valami oka annak, hogy miért vannak folyton jelen az endokannabinoidok”.
5 meglepő dolog amit tudni érdemes az Endokannabinoid Rendszerről
Mi van a fűben?
A kutatók úgy jellemezték az endokannabinoid rendszert, mint a legbonyolultabb és mindenhol jelenlévő szignalizációs (jelátviteli) rendszert az emberi szervezetben, annak ellenére, hogy az 1980-as évekig senki sem tudta, hogy ez a humán élettan része. A felfedezés egy szokatlan forrásból származott – történetesen a gyakran nevetség tárgyává is tett erőfeszítésből, hogy megértsék a kannabisz szervezetre gyakorolt pszichotikus hatását.3
1964-ben kutatók szerették volna megtalálni a kannabisz növény pszichotróp komponensét, amit később THC-ként azonosítottak.4
Több mint két évtizeddel később, 1988-ban megtalálták az első közvetlen bizonyítékot egy endogén szignalizációs rendszerre a THC-val kapcsolatban – patkány modell agyában egy receptorra bukkantak, ami a THC szintetikus alakját képes nagy affinitással kötni.5 Emberben ennek a receptornak egy kémiai antagonistával való gátlása hatékonyan megakadályozza a kannabiszfogyasztás során tapasztalt pszichotikus élményt.
A receptort (CB1) utólag sikerült azonosítani más emlősök agyában is (beleértve az embert), és úgy találták, hogy hasonló denzitásban (sűrűségben) van jelen, mint a többi neurotranszmitter receptor, például glutamát, GABA és dopamin receptorai.6 Egy másik kannabinoid receptor, a CB2 1993-ban került felfedezésre.7 Ezt a receptort először patkány lépéből sikerült izolálni. Ez a megdöbbentő felfedezés volt az előjele annak, hogy további felfedezésre váró terület van még, példának okáért az, hogy az endokannabinoid rendszer távol az agytól, a szervezet minden részén ellátja feladatait.
Ezeknek a receptoroknak a jelenléte arra ösztönözte a kutatókat, hogy megkeressék a hozzájuk kötődő természetes ligandokat. Az első endokannabinoid, amit azonosítottak, egy zsírsav-alapú (lipofil) agonista volt, mely mindkét receptorral képes kölcsönhatni. Az anandamid nevet kapta, ami a szanszkrit ananda (belső boldogság) szóból ered. A második agonista, a 2-AG nem kapott olyan klassz nevet, mint az anandamid, de elmondható, hogy nagy mennyiségben van jelen az emlősök agyában fiziológiás állapotban.
1995-re az ún. „grass route” kiteljesedett: Három évtized alatt a kutatók azonosították a THC-t, az endogén receptorait és e receptorok endogén ligandjait. Maccarrone úgy véli, hogy az endokannabinoidok a legrégebbi jelátviteli molekulák közé tartoznak, amelyet az eukarióta sejtek használnak. Csapata nemrég bemutatta, hogy az anandamid és a hozzá kapcsolódó enzimek a szarvasgombában is jelen vannak. Ez az ízletes gomba kb. 156 millió évvel ezelőtt jelent meg a Földön, ami azt feltételezi, hogy az endokannabinoidok a kannabisz növénynél korábban alakultak ki.8
„Olyanok, mint egy fő jelátviteli rendszer, aminek a lipidjeivel a többi szignál megtanult kommunikálni” – állítja Maccarrone. Az agyban az endokannabinoidok és egyéb neurotranszmitterek képesek kölcsönösen hatni egymásra. A reproduktív rendszerben a szteroid hormonokkal, az izmokban a myokinekkel, stb.
Annak ellenére, hogy a kutatók dokumentálták az endokannabinoid rendszer létezését test szerte, továbbra sem tudják biztosan, hogy milyen szerepet játszik az agyon kívüli területeken, ahol a szinaptikus jelátvitelben és plaszticitásban vesz részt. Az egészséges, nem elhízott állatokban jellemzően nem találtak összefüggést az endokannabinoid receptorok génjének kiütésével a periférián lévő szervekben. „Nincs semmilyen érzékelhető hatása egyik fontos biológiai funkcióra sem” – állítja Kunos György, a NIAAA (National Institute on Alcohol Abuse and Alcoholism) tudományos direktora.
Mi ez a nyüzsgés?
Ennek a funkcionális fekete doboznak az egyetlen kivétele a gasztrointesztinális traktus. Az a felvetés, miszerint a kannabisz – bővebben az endogén kannabinoidok – hatással van a bélrendszerre nem meglepő. A kannabisz növényből származó készítményeket régóta alkalmazzák emésztőrendszeri panaszok kezelésére, beleértve a bél gyulladásos megbetegedését és a hányást. Még mielőtt a CB1-et felfedezték volna, a kutatók felvetették, hogy a kannabinoidok szabályozzák a gasztrointesztinális traktus motilitását – az izmok összehangolt működését, amely a táplálék keverését és továbbítását szolgálja a beleken keresztül. Példának okáért, 1973-ban ausztrál kutatók igazolták egérmodellen, hogy a THC szájon át történő bevitele lelassította a táplálék áthaladását a bélrendszeren.9 Ennek megfelelően a rendszer egyes részeinek kiütése összefüggésbe hozható a táplálék megnövekedett mozgásával a vastagbélszakaszon keresztül, amely általános tünete az irritábilis bélszindrómának (IBS). Ezek a pályák konzerváltan vannak jelen több fajban is.10
Mind a CB1 és CB2 receptorok aktívan jelen vannak a bélben, jóllehet, hogy a bél különböző funkcióiban is érintettek. A Calgary Egyetemen, Keith Sharkey és kollegái azt találták, hogy a gyulladásban lévő bélben megfigyelhető megnövekedett intesztinális motilitás visszafordítható, ha a CB2 receptorokat aktiválják (a CB1 esetében ez nem mondható el).11
„Elérkeztünk ahhoz a ponthoz, amikor is meg kell értenünk, hogy az endokannabinoidok hogyan lehetnek ilyen széles körben relevánsak – történetesen a szervezet minden részén – állítja Mauro Maccarrone, a római Campus Bio-Medico Egyetem professzora.
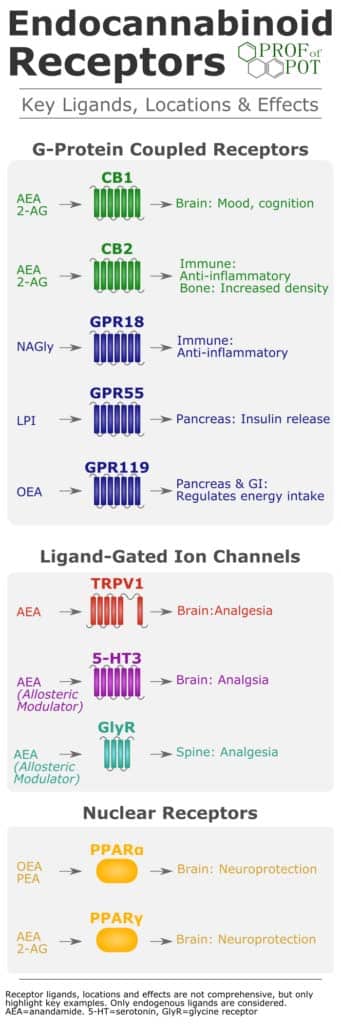
A helyzetet tovább bonyolítja, hogy van egy csomó nem-klasszikus kannabinoid receptor is a bélben, amelyek kölcsönhatásba lépnek az endokannabinoidokkal, állítja Jakub Fichna, a lengyel Lodzi Orvosi Egyetem biokémiai intézetének vezetője. Laboratóriumában vizsgálták ezeknek a receptoroknak a működését gyulladásos bélbetegségekben (IBD és IBS). A bél állapotától függően néhány ilyen nem-klasszikus receptornak agonistára vagy antagonistára sincs szüksége ahhoz, hogy aktivizálódjon. Fichna szerint „Ezt okozhatja a nyomás vagy a pH megváltozása a receptorok környezetében. Példának okáért, gyulladás esetén csökkenő pH figyelhető meg, és ez bőven elég ahhoz, hogy néhány endokannabinoid receptor aktívvá váljon.”
Az endokannabinoidok és receptoraik úgy tűnik, hogy a gasztrikus szekrécióban, ion transzportban, sejt proliferációban is részt vesznek a bélrendszeren belül. Továbbá az étvágyban. A kannabisz használók gyakran óriási éhségérzetet tapasztalnak („munchies”) – hirtelen és azonnali étvágynövekedés, miután cigaretta formában elszívják vagy lenyelik az anyagot. Kunos szerette volna megtudni, vajon az endokannabinoidok okozzák-e ezt az étvágynövekedést. 2001-ben közreműködő munkatársak segítségével igazolta a gyanút: az endokannabinoidok hatással vannak a CB1 receptorokra, ezáltal étvágyat kelt. Megfigyelték továbbá, hogy azok az egerek, amelyeknek CB1 receptora kiütésre került kevesebbet ettek, mint vad típusú társaik.12
A kiegészítő vizsgálatok megerősítették azt a feltevést, hogy az endokannabinoidok egy általános étvágyfokozó jelként működnek. Ahogy DiPatrizio munkája is bemutatta, az endokannabinoidok szabályozzák a táplálék felvételét, azonban nem kizárólagosan az agyon keresztül, hanem a bélrendszerben létrehozott szignálokon segítségével. Ez egy egyszerű feltételezés, mégis nagy jelentőséggel bír az elhízás és egyéb anyagcsereproblémák kezelésében.
A posztdoktori képzése alatt DiPatrizio úgy találta, hogy mikor a rágcsálók megízlelték a zsíros táplálékot (csak ízlelték, nem nyelték le) az endokannabinoidok szintje megnövekedett a patkányok vékonybelében – és sehol máshol a szervezetben. Mikor a CB1 receptor szignalizációt egy antagonistával blokkolták, az a rágcsálók zsíros táplálék bevitelének csökkenéséhez vezetett. „Ez azt sugallja, hogy ez egy nagyon fontos és kritikus mechanizmus, ami táplálékfelvételhez vezet,” állítja DiPatrizio.
Evolúciós szempontból nézve, van értelme annak, hogy a zsír felvételéhez a szervezet egy pozitív feedback mechanizmussal rendelkezik. A vadonban, mikor egy állat magas-energiatartalmú táplálékot észlel, azt hasznos, hogy elraktározza. Azonban ez már nem igaz a mai fejlett társadalmakban élő emberekre. „Ott már nincs éhínség. Jellemző az állandósult dőzsölés, így ez a rendszer túlfogyasztáshoz vezethet”, állítja DiPatrizio.
Sharkey úgy tekint erre a rendszerre, mint a szervezeten belüli homeosztázis (belső egyensúly) szabályozójára, különösen figyelembe véve a táplálék felvételének, testsúlynak és a gyulladásnak a szabályozásának fenntartását. „Nagyon fontosnak tűnik az energia konzerválásában,” állítja Sharkey. „Ám főleg a modern, nyugati társadalmakban, ezek azok a dolgok, amelyek szabályozása zavart szenvedett.”
A bajos idők
Habár az endokannabinoid rendszer feladatait az egészséges szövetekben (az agyon és bélrendszeren kívül) még mindig titkok övezik, a betegségek vezethetnek nyomra. Elhízás során, a CB1 és CB2 receptorok az egész szervezetben felülszabályozottak, beleértve a májat és a zsírszövetet is. A CB1 receptorok aktivációja táplálék bevitel esetén nő, hatással van az energia anyagcserére a perifériális szövetekben. A 2-es típusú cukorbetegségben az endokannabinoidok és receptoraik felülszabályozottak a keringő makrofágokban és hozzájárulnak a hasnyálmirigy béta sejtjeinek pusztulásához, amelyek raktározzák és felszabadítják az inzulint.
Érdekes módon, a tartós kannabisz fogyasztók körében nem bizonyított a cukorbetegség vagy az elhízás nagyobb arányú kialakulása. Kutatók szerint a folyamatos használat a CB1 receptorok alulszabályozottságát eredményezheti – a farmakológiai tolerancia egy formáját. Egy másik lehetőség, amelyet Sharkey és munkatársai fedeztek fel 2015-ben az, hogy a tartós THC felvétel megváltoztatja a bél mikrobiomját, ami hatással van a táplálék felvételére és megakadályozza a testsúly növekedését.13 Májbetegség esetén a CB1 felülszabályozottsága hozzájárulhat a sejthalálhoz a sebszövet felhalmozódásához (fibrózis).14
Az még viszont vita tárgya, hogy mindig az endokannabinoid receptorok-e a rosszfiúk a betegségek kialakulásában. Néhány esetben az endokannabinoid szignalizáció terápiás hatásúnak bizonyult. Állatmodellekkel bizonyítva az endokannabinoidok hatásos fájdalomcsillapítók és az endokannabinoid rendszernek gyulladáscsökkentő tulajdonságai is vannak bizonyos körülmények között. IBD-ben Sharkey csapata úgy találta, hogy mind a CB1 és CB2 receptorok aktivációja a gyulladás csökkenését eredményezte, azt a látszatot keltve, hogy ez a rendszer egy védőerőt képez. Hasonlóképpen a CB2 aktivációja is gyulladáscsökkentőnek bizonyult atherosclerosis (ütőér elmeszesedés) esetében, O’Sullivan szerint, aki a karidovaszkuláris rendszeren belül kutatja az endokannabinoidokat. „Egy kicsit olyan, mint egy mentő receptor,” mondja. „Betegség esetén felülszabályozottak”. Számos tanulmány állítja, hogy a kannabinoidok – növényből származó vagy olyan szintetikus molekulák, amelyek utánozzák mind a botanikai mind a szervezet saját kannabinoidjait – közvetlenül gátolhatják a tumornövekedést, azáltal, hogy a tumorsejtek halálát idézi elő.
De az, ami az endokannabinoid rendszert ennyire érdekessé teszi az az, hogy mindenütt jelen van, és más-más szereppel bír a szervezeten belül – ezért ennyire bonyolult gyógyszercélpont. Az elmúlt tíz évben, két olyan gyógyszerről, ami az endokannabinoid rendszert célozta bebizonyosodott, hogy szörnyű mellékhatásokat produkál ember esetében, ha a vegyület átlépi a vér-agy gátat. A célhelyet elkerülő hatások más szervek esetében is hosszútávú következményekkel járhatnak, úgy, mint például fiatal nők esetében a reproduktív rendszer károsodása. Jelenleg 18 különböző CB2 ligand újkeletű gyógyszertani vizsgálata zajlik, mint lehetséges gyógyszerjelölt. Maccarrone és európai kutatók egy nagy csoportja, a Rocheval együttműködve arra a következtetésre jutott, hogy a vegyületekből csak 3 (Roche által fejlesztettek közül egyik sem) érdemes a további preklinikai vagy klinikai tanulmányokra.15 A többi vegyület nagy része túl sok célhelyet tévesztő hatást okozott.
A kutatók napjainkban tovább dolgoznak, annak érdekében, hogy olyan második-generációs gyógyszereket fejlesszenek, amelyek sokkal specifikusabban célozzák meg a perifériás rendszert. „Ha a kutatók közössége szembenéz azzal a kihívással, hogy ténylegesen megértse azt, hogy bizonyos gyógyszerek hogyan célozzák meg a megfelelő célpontot, akkor csodálatos gyógyszereket készíthetünk a jövőben,” állítja Maccarrone. A vegyületek nagy része még preklinikai fázisban tart, ámbár Kunos reméli, hogy az amerikai Élelmiszer-biztonsági és Gyógyszerészeti Hivatal (FDA) hamarosan elfogadja, mint kísérleti új gyógyszer (IND) azt az anyagot, amin a csapatával dolgoztak, mint a nem-alkoholfüggő májzsírosodás lehetséges gyógyszere. A vegyület nem jut el az agyhoz, és úgy tervezték, hogy a májban halmozódjon fel, amely magyarázat a májbetegség hatékony kezelésére anélkül, hogy elmegyógyászati mellékhatásokat okozna állatmodelleken, állítja Kunos.16
Ha a kutatóknak sikerül kitalálniuk, hogyan kerüljék el a pusztító, célhelyet tévesztő mellékhatásokat, akkor az endokannabinoidok hatékonyan segíthetnek a betegségek kezelésében, mivel közvetett kapcsolatot biztosítanak az aggyal. „Egy ideje már tudjuk, hogy az agy képes szabáyozni a bélrendszert,” állítja Sharkey. Endokannabinoidok segítségével úgy tűnik, hogy a bél is képes módosítani az agy működését. Ma már egyértelmű, hogy például a bél perifériás idegeiből eredő nagyon aktív kommunikációt folytató útvonalai képesek az agy funkcióit szabályozni. Számtalan tanulmány bizonyítja, hogy a vagus ideg a fő információs szupersztráda a bél és az agy között.
DiPatrizio ezeket a kommunikációs útvonalakat tanulmányozza és reméli, hogy sikerül megtalálni a táplálkozás szabályozásának módjait anélkül, hogy az agyat bármilyen gyógyszerrel befolyásolnánk. A kutatást kiegészítették további bizonyítékokkal, amelyek azt igazolják, hogy a bél képes szabályozni a gyulladáskeltő citokineket a vérben és a központi idegrendszer rendellenességeit is befolyásolják.
„Úgy hisszük, hogy képesek vagyunk biztonságosan irányítani az agyat és a belet külön-külön,” állítja DiPatrizio. „És ez az, amiért az endokannabinoid receptorok olyan vonzó célpontok.”
Kérünk mindenkit, támogassa non-profit egysületünk munkáját, akár csak egy pohár kávé árával.
Ezen az oldalon lehet támogatást küldeni:
https://orvosikannabisz.com/tamogatas/
Hivatkozások:
- N.V. DiPatrizio et al., “Endocannabinoid signal in the gut controls dietary fat intake,” PNAS, 108:12904-08, 2011.
- D.A. Argueta, N.V. DiPatrizio, “Peripheral endocannabinoid signaling controls hyperphagia in western diet-induced obesity,” Physiol Behav, 171:32-39, 2017.
- I. Katona, T.F. Freund, “Multiple functions of endocannabinoid signaling in the brain,” Annu Rev Neurosci, 35:529-58, 2012.
- Y. Gaoni, R. Mechoulam, “Isolation, structure, and partial synthesis of an active constituent of hashish,” J Am Chem Soc, 86:1646-47, 1964.
- W.A. Devane et al., “Determination and characterization of a cannabinoid receptor in rat brain,” Mol Pharmacol, 34:605-13, 1988.
- M. Herkenham et al., “Cannabinoid receptor localization in brain,” PNAS, 87:1932-36, 1990.
- S. Munro et al., “Molecular characterization of a peripheral receptor for cannabinoids,” Nature, 365:61-65, 1993.
- G. Pacioni et al., “Truffles contain endocannabinoid metabolic enzymes and anandamide,” Phytochemistry, 110:104-10, 2015.
- G.B. Chesher et al., “The effect of cannabinoids on intestinal motility and their antinociceptive effect in mice,” Br J Pharmacol, 49:588-94, 1973.
- N.V. DiPatrizio, “Endocannabinoids in the gut,” Cannabis Cannabinoid Res, 1:67-77, 2016.
- R. Mathison et al., “Effects of cannabinoid receptor-2 activation on accelerated gastrointestinal transit in lipopolysaccharide-treated rats,” Br J Pharmacol, 142:1247-54, 2004.
- V. Di Marzo et al., “Leptin-regulated endocannabinoids are involved in maintaining food intake,” Nature, 410:822-25, 2001.
- N.L. Cluny et al., “Prevention of diet-induced obesity effects on body weight and gut microbiota in mice treated chronically with Δ9-tetrahydrocannabinol,” PLOS ONE, 10:e0144270, 2015.
- P. Pacher et al., “The endocannabinoid system as an emerging target of pharmacotherapy,” Pharmacol Rev, 58:389-462, 2006.
- M. Soethoudt et al., “Cannabinoid CB2 receptor ligand profiling reveals biased signalling and off-target activity,” Nat Commun, 8:13958, 2017.
- R. Cinar et al., “Hybrid inhibitor of peripheral cannabinoid-1 receptors and inducible nitric oxide synthase mitigates liver fibrosis,” JCI Insight, 1:e87336, 2016.
- R. Christensen et al., “Efficacy and safety of the weight-loss drug rimonabant: A meta-analysis of randomised trials,” Lancet, 370:1706-13, 2007.