Kanadai orvosok ajánlásai a kannabinoidok titrálásához és az opioidok csökkentéséhez krónikus fájdalomcsillapítás esetén

The International Journal of Clinical Practice
A kannabinoid alapú termékeket felíró orvosoknak konkrét útmutatásokra van szükségük, amelyeket valós talapasztalatokkal rendelkező orvosok dolgoztak ki.
Az újonnan megjelent „Konszenzuson alapuló ajánlások a kannabinoidok titrálásához és az opioidok csökkentéséhez krónikus fájdalomcsillapításra” kiváló példa, amiben kanadai orvosok ajánlásokat dolgoztak ki a következőkről:
- Mikor érdemes megfontolni a kannabinoidok bevezetését krónikus fájdalommal küzdő betegeknél, akik opioidokat szednek?
- Hogyan lehet bevezetni a kannabinoidokat krónikus fájdalommal küzdő betegeknél, akik opioidokat szednek?
- Mikor és hogyan lehet az opioidokat csökkenteni a kannabinoidokat szedő krónikus fájdalommal küzdő betegeknél?
- A klinikai eredmények értékelése, valamint a betegek felügyeletének és biztonságának irányítása
Algoritmus röviden:
- Krónikus fájdalom esetén opioidokat szedő betegeknél, akik nem érik el a kezelési célokat, fontolóra lehet venni a kannabinoid alapú termékek használatát.
- Kezdjük CBD domináns orális kivonattal nappal, és fontoljuk meg a THC hozzáadását.
- A THC hozzáadásakor kezdjük el 0,5–3 mg-mal, és emeljük 1-2 mg-mal hetente egyszer vagy kétszer, maximum napi 30–40 mg-ig.
- Kezdjük el az opioid csökkentését, amikor a beteg kisebb vagy nagyobb javulásról számol be, kevesebb “szükség esetén” használt gyógyszerre van szüksége a fájdalom visszaszorítására, és/vagy a kannabisz adagját optimalizálták.
- Az opioid csökkentése 1–4 hetente a morfin ekvivalens dózis (MED) 5–10%-a lehet.
- A klinikai siker meghatározható a funkció/életminőség javulásával, a fájdalom intenzitásának ≥30%-os csökkentésével, az opioid dózis ≥25%-os csökkentésével, az opioid dózisának csökkentésével <90 mg MED-ig és/vagy az opioidokkal kapcsolatos nemkívánatos események csökkenésével
Bár nehéz lesz ilyen kannabinoid alapú termékprotokollokat kifejleszteni minden betegség esetén, a hasonló algoritmusok nagyon szükséges útmutatást nyújtanak az orvosoknak és megkönnyítik a betegek életét.
Kiegészítés – Nemzetközi ajánlások orvosi kannabisz adagolásához és beadásához krónikus fájdalom kezelésére:
Ajánlások orvosi kannabisz adagolásához és beadásához krónikus fájdalom esetén
Algoritmus bővebben:
1. Mikor érdemes megfontolni a kannabinoidok bevezetését krónikus fájdalommal küzdő betegeknél, akik opioidokat szednek?
Az első tartomány olyan betegtényezőkről tett fel kérdéseket, amelyek befolyásolhatják a beteg alkalmasságát kannabinoidokkal történő kezelésre. A legfontosabb konszenzusos megállapítások a következők:
1. Ha a beteg kórtörténetében pszichózis szerepel, terhes vagy szoptat, vagy ha a kannabinoidokra korábban kedvezőtlen reakciót váltottak ki nála, kerülni kell a kannabinoidokat. Bár a pszichózis kórtörténetével rendelkező beteg esetében a THC tűnik a legjelentősebb károkozónak, és a CBD valójában csökkentheti a pszichózist. Az orvosok megfontolhatják az orvosi kannabiszt egy páciensnél, aki: opioidokat szed bármely morfin ekvivalens dózisban (MED), nem éri el a krónikus fájdalomcélokat, az opioidokkal kapcsolatos káros hatások tapasztal és/vagy az opioidokkal kapcsolatos károk kockázati tényezőit mutatja. Fontos megjegyezni, hogy ennek a konszenzusos kezdeményezésnek nem célja azt javasolni, hogy minden opioidot szedő beteg csökkentse az opioidokat. Egy nemrégiben készült kommentárban pontosították a CDC (amerikai Járványvédelmi és Járványmegelőzési Központ) iránymutatásait az opioid csökkentésről annak kiemelésére, hogy a klinikusoknak kerülniük kell az opioid-dózis ≥90 MED-re történő emelését, de nem feltétlenül hagyják abba az opioidok alkalmazását a nagy dózist kapó betegeknél. A párbeszéd és a döntéshozatal megosztása a pácienssel, valamint az opioidok csökkentésével és abbahagyásával járó előnyök és kockázatok körültekintő értékelése erősen ajánlott. Ezenkívül bármilyen további gyógyszerészeti beavatkozás bevezetése előtt meg kell próbálni és maximalizálni kell a bizonyítékokon alapuló pszichológiai és fizikoterápiás beavatkozásokat az opioidhasználat csökkentése érdekében.
2. Egyetértés volt abban, hogy a CBD vagy a THC használatára nincs korhatár korlátozás. A CBD vonatkozásában a csoport gyorsan konszenzusra jutott, mivel a CBD nagy dózisai biztonságosnak bizonyultak gyermekeknél, bár olyan betegeknél, akik nem hasonlítanak a krónikus fájdalommal járó tipikus betegekhez. Ezzel szemben vita folyt a minimális életkorra vonatkozó ajánlás körül a THC esetében. A THC alkalmazásakor gondosan mérlegelni kell a fiatalabb populációt, mivel az idegrendszer csak 25 éves koráig fejlődik ki teljesen. A konszenzusos csúcstalálkozó résztvevői azonban arról vitatkoztak, hogy ha egy fiatal beteg már opioidokat szed, akkor nem tűnik ésszerűnek a kannabinoid terápia visszatartása, amíg egy adott életkorna lépnek. Hasonlóképpen, bár nem állapodtak meg a maximális életkorban, körültekintő figyelmet kell fordítani a kannabinoidok időskorúak kezelésében történő mérlegelésére, ugyanakkor fel kell ismerni, hogy az idős emberek különösen érzékenyek az opioidok káros hatásaira.
2. Hogyan lehet bevezetni a kannabinoidokat krónikus fájdalommal küzdő betegeknél, akik opioidokat szednek?
A második tartomány kérdéseket tett fel a kannabinoidok opioidok jelenlétében történő beadásának, bevezetésének, titrálásának és adagolásának kérdésével kapcsolatban. A legfontosabb konszenzusos megállapítások a következők:
1. Egyetértés volt abban, hogy a kannabinoidok beadásának előnyös formája az orális út, olajkivonatok vagy kapszulák alkalmazásával. Szublingvális tinktúrák is szóba jöhetnek. Konszenzus született arról, hogy határozottan ellenzik a kannabisz elszívását. Óvatosan kell eljárni azokban a joghatósági területeken, ahol a szabályozott és szabványosított kannabisz termékek nem állnak rendelkezésre.
2. Megállapodás született abban, hogy napközben a betegek CBD szájon át történő adagolását 5–20 mg tartományban kell megkezdeni. A THC esetében egyetértés volt abban, hogy a kezdeti dózistartománynak 0,5–3 mg-nak kell lennie, majd 1–2 mg-mal kell titrálni 1–2 hetente a krónikus fájdalomcélok elérése érdekében.
3. Éjszakai használat esetén nem volt konszenzus a CBD vagy a THC dózisáról, vagy a THC:CBD eloszlási arányról, bár megvitatták a THC potenciális fontosságát az alvás minősége szempontjából, amely támogathatja a krónikus fájdalomcsillapítást.
4. Áttörő fájdalom esetén a szárított kannabisz virág elpárologtatása ajánlott. Fontos megjegyezni, hogy a párologtatott szárított virág eltér az elektronikus cigaretta eszközön keresztüli gőzöléstől. A szárított virág elpárologtatása ideális esetben jóváhagyott orvostechnikai eszközökkel valósul meg, bár sokféle, eltérő minőségű párologtatót lehet használni. Ezzel szemben a kannabisz elektronikus cigaretta eszközökkel történő elpárologtatása a beteget nem biztonságos adalékanyagoknak teheti ki és növelheti az új tüdőbetegség, az EVALI (e-cigaretta vagy gőzölgő termék használatához kapcsolódó tüdősérülés) kockázatát. Amíg az elektronikus cigarettaeszközök nem bizonyulnak biztonságosnak, az orvosi kannabisz áttöréses fájdalomra történő belélegzését kizárólag orvosilag engedélyezett párologtatókkal kell elvégezni, szárított kannabisz virágok használatával.
3. Mikor és hogyan lehet az opioidokat csökkenteni a kannabinoidokat szedő krónikus fájdalommal küzdő betegeknél?
A harmadik terület megvitatta az opioidok csökkentésének idejét és módját azoknál a betegeknél, akiknél opioidokat és kannabinoidokat kaptak. A legfontosabb konszenzusos megállapítások a következők:
1. A pácienstől függően kezdje el az opioidok csökkentését, ha az alábbi kritériumok bármelyike teljesül: a beteg javult a fájdalomban/funkcióban; optimalizálták a kannabinoid adagját; vagy a beteg kevesebbszer használ „szükség esetén” gyógyszert. Fontos, hogy azt javasolták, hogy ne kezdjék el csökkenteni az opioidok mennyiségét a kannabinoid indításakor vagy meghatározott kannabinoid dózisnál.
2. Az opioidcsökkentés megkezdésekor 1–4 hétenként fokozatos opioiddózis-csökkentést állapítottak meg a morfin ekvivalens dózis (MED) 5–10%-ával. A dóziscsökkentés gyakoriságának ütemterve széles, hogy lehetővé tegye a betegek testreszabását, és hasonló a korábban publikált opioidcsökkentő ajánlásokhoz. Újabban az Egyesült Államok Egészségügyi és Humánügyi Minisztériuma közzétette az opioidcsökkentés iránymutatásait. Ezek az irányelvek nem határoznak meg konkrét MED-célokat, és ösztönzik az egyénre szabott opioidcsökkentést megközelítést és a pácienssel közös döntéshozatalt. Valójában lehetnek olyan betegek, akiknél a célkitűzéseiktől és szükségleteiktől függően 20–50%-os gyors csökkentést is alkalmazhatnak hatékony kannabinoid dózisra való titrálás után.
4. A klinikai eredmények értékelése, valamint a betegek felügyeletének és biztonságának irányítása
A negyedik terület az opioidokat és kannabinoidokat szedő krónikus fájdalommal küzdő betegek monitorozásával, biztonságával és a hatékonyság mérésével kapcsolatos kérdéseket vizsgálta. A legfontosabb konszenzusos megállapítások e területen:
1. Az opioidok és a kannabinoidok együttes alkalmazásának korai szakaszában azt javasolták, hogy havonta egyszer vagy kétszer kövessék után a betegeket, amíg a beteg nem stabil. Megállapodás született abban, hogy miután az egészségügyi szakember és a beteg komfortos, az utánkövetés 3 havonta történhet. Megállapodás született abban is, hogy ezeknek a betegeknek a monitorozását a kezelőorvostól eltérő egészségügyi szakemberek is vezethetik, és hogy ezeket az utánkövetéseket telefonon vagy otthoni látogatáson keresztül is el lehet végezni, attól függően, hogy mi működik a legjobban az egészségügyi szakember és a beteg számára. Ezen a ponton, annak ellenére, hogy a beteg stabil lehet a krónikus fájdalomcsillapításában, az orvosi kannabisz beadásának és adagolásának változtatására lehet szükség az optimális fájdalomkontroll érdekében.
2. Az opioidokat és a kannabinoidokat egyaránt szedő betegek biztonságának mérlegelésekor az egészségügyi szakembereknek szűrniük kell opioid elvonást, az illegális opioidhasználatot, a kannabinoidokkal kapcsolatos mellékhatásokat, más tiltott szerek használatát és a pszichózis tüneteit. A kannabinoid-titrálást le kell állítani: ha a páciens céljai teljesülnek; amikor a kannabinoid-kezelés eléri a hatékonysági platót (azaz a dózis növelése után nincs változás a fájdalomcsillapításban); vagy ha a beteg kannabinoiddal összefüggő nemkívánatos eseményt tapasztal. Ha a páciens kannabinoiddal összefüggő nemkívánatos eseményt tapasztal, javasoljuk a társított kannabinoid dózisának csökkentését. Megállapodás született abban, hogy ha a betegnél opioid elvonási tünetek jelentkeznek, akkor az egészségügyi szakembernek fontolóra kell vennie az opioidcsökkentés lassítását vagy szüneteltetését.
3. A kezelés sikerének mérlegelésekor nem találtak konszenzust abban, hogy a hatékonyság megállapításához validált kérdőívet kell-e használni. Egyetértés volt azonban abban, hogy indítsák el és dokumentálják a kezelés során a beteggel folytatott megbeszéléseket a fájdalomcsillapítás mértékéről, az alvás minőségéről és a mindennapi funkcionalitásról. Ezzel egyetértésben abban állapodtak meg, hogy a kannabinoidok titrálásának és az opioidok csökkentésének klinikai sikerét a beteg funkciójának javulása határozza meg legegyértelműbben.
Teljes útmutatás itt olvasható: https://onlinelibrary.wiley.com/doi/full/10.1111/ijcp.13871
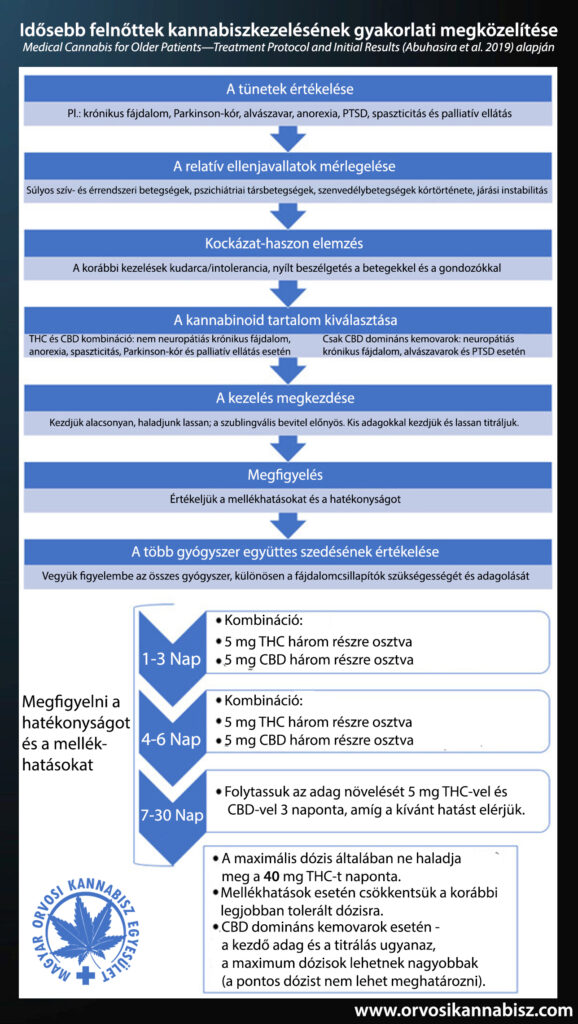
Idősebb felnőttek kannabiszkezelésének gyakorlati megközelítése (2019): https://pubmed.ncbi.nlm.nih.gov/31683817/
Kérünk mindenkit, támogassa non-profit egysületünk munkáját, akár csak egy pohár kávé árával.
Ezen az oldalon lehet támogatást küldeni:
https://orvosikannabisz.com/tamogatas/
Visszanyert én: A kannabisz fájdalomcsillapító hatásának fenomenológiai vizsgálata











