Klinikai tanulmány gyerekekkel: Kannabisz alapú gyógyszer csökkenti az epilepsziás rohamokat
Egy kannabiszból származó kísérleti gyógyszer sikeresen csökkenteni az epilepsziás rohamokat az első nagy klinikai vizsgálatban, jelentette be a termék fejlesztője március elején.
A GW Pharmaceuticals szerint a gyógyszer, az Epidiolex, elérte a vizsgálat fő célját, csökkentette a epilepsziás rohamok számát a placebóhoz képest Dravet szindrómánál, az epilepszia egy ritka formájánál. Aznap a GW részvények több, mint kétszeresére ugrottak.
Ha az Epidiolex megkapja a hatósági jóváhagyást, ez lenne az első receptre kapható gyógyszer az Egyesült Államokban, amit csak kannabiszból készül. A készítmény egy kannabidiolt (CBD) tartalmazó folyadék. A GWP42003 néven is ismert belsőleges oldat egy olajos oldat, amiben 100 mg/ml kannabidiol (CBD) van feloldva segédanyagokban, szezámolajban, etanolban, szukralózban és eper aromában.
A GW szerint a közel 500.000 amerikai epilepsziás gyerekek legalább 30%-ánál nem használnak a hagyományos gyógyszerek. Néhány ilyen gyermek szölői rászánták magukat, hogy kipróbálják a kannabisz kivonatokat, amiket az orvosi kannabisz gyógyszertárak kínálnak.
Válaszul a szülők nyomására számos amerikai államban hoztak olyan törvényeket, amik megkönnyítik a kannabisz alapú termékekhez való hozzérést. És néhány család “kannabisz menekülté” vált, Coloradoba költöztek, ahol könnyebb megszerezni az ilyen kivonatokat.
Több száz gyermekek és fiatal felnőtt használ Epidiolex-et a klinikai vizsgálatokon kívül, olyan programok keretében, amelyek lehetővé teszik a kétségbeesett betegek számára a kísérleti gyógyszerekhez való hozzáférést.
Bár sok szülő számolt jelentős rohamcsökkentésről, a szakértők óvatosságra intenek az anekdotikus beszámolókkal kapcsolatban, mondván, hogy az ilyen kezeléseket szükséges placebóval összehasonlítani, hogy megbizonyosodjunk arról valóban működnek-e. Azért a GW kísérletét érdemes szoros figyelemmel követni.
“Nagyon büszke és boldog vagyok ezzel a tanulmánnyal, mert a tudomány – úgy csináltuk a dolgokat, ahogy azokat csinálni kell,” mondta a tanulmány vezető kutatója, Dr. Orrin Devinsky az Átfogó Epilepszia Központ New York-i Egyetemén a Langone Egészségügyi Központban adott interjúban. “Határozottan javaslom, hogy az Egyesült Államokban végezzünk átfogó orvosi kannabisz értékelést.”
A vizsgálatban 120 beteg szerepelt, akiknek átlagéletkora 10 év volt és átlagosan 13 epilepsziás rohamuk volt egy hónapban a tanulmány elején, annak ellenére, hogy átlagosan három gyógyszert szedtek egyszerre. A gyerekek fele véletlenszerűen a CBD gyógyszert és a másik fele placebot kapta, a már meglévő epilepszia gyógyszerek mellett.
A cég azt mondta, hogy azoknak a betegekeknek a rohamgyakorisága akik Epidiolex-et kaptak, 39 százalékkal csökkentek az 14 hetes kezelési periódusban, szemben a négy hétes periódussal a kezelés kezdete előtt. Azoknál akik placebo kaptak, a csökkenés 13 százalék volt. A különbség a két csoport között statisztikailag szignifikáns volt.
Nyolc Epidiolex-et és egy placebót kapó beteg mellékhatások miatt abbahagyta a kezelést. A leginkbb előforuló mellékhatások az álmosság, a hasmenés, a csökkent étvágy, a fáradtság, a láz, a hányás és felső légúti fertőzés volt. De a GW azt mondta, hogy a gyógyszert jól tolerálták.
Klinikai vizsgálatban a kannabisz kivonat csökkenti a gyermekkori epilepsziás rohamok számát
“Ennek az Epidiolex vizsgálatnak az eredményei fontosak és izgalmasak, ezek az első placebo-kontrollos bizonyítékok a gyógyászati kannabidiol biztonságosságáról és hatásosságáról Dravet szindrómás gyermekeknél, ami az egyik legsúlyosabb és legnehezebben kezelhető-típusú epilepszia”, mondta Dr. Devinsky. “Ezek az adatok azt mutatják, hogy az Epidiolex klinikailag jelentős csökkenést mutat a rohamok gyakoriságában, elfogadható biztonságossági és tolerálhatósági profillal, amely az epilepszia közösségnek egy megfelelően standardizált és tesztelt gyógyászati kannabidiolt tesz elérhetővé receptre kapható formában.”
“A 3. fázisú klinikai vizsgálat pozitív kimenetele egy jelentős mérföldkő az Epidiolex fejlesztésében, mint potenciális új kezelés Dravet szindrómától szenvedők számára. Izgatottan várjuk, hogy az Epidiolex lehet az első FDA által jóváhagyott kezelési lehetőség kifejezetten Dravet szindrómás betegeknek és családjaiknak,” mondta Justin Gover, a GW vezérigazgatója.
A vizsgálat teljes részleteit nem hozták nyilvánosságra; a cég azt mondta, hogy azokat egy orvosi konferencián fogják bemutatni.
A GW, ami egy londoni székhelyű cég, azt mondta, hogy találkozózt szervez az FDA-vel (Amerikai Gyógyszer- és Élelmiszerellenőrző Hatóság), hogy megvizsgálják, vajon az Epidiolex megkaphatja-e a jóváhagyást egyetlen tanulmány alapján. Egy másik Dravet szindróma vizsgálat eredményeit későbbre várják még idén, valamint két vizsgálat eredményeit az epilepszia egy másik formájáról, amit Lennox-Gastaut szindrómának hívnak.
Nincsenek kifejezetten Dravet szindrómára jóváhagyott gyógyszerek, ami általában csecsemőkorban kezdődik és mintegy 5000 gyereket érint az Egyesült Államokban. Még nem ismert, hogy az Epidiolex segíthet-e a járás és az értelmi fogyatékosság területén, ami a Dravet szindrómával járhat, mondta Dr. Devinsky.
Ha az Epidiolex-et jóvá is hagyják, néhány szülő valószínüleg kitart az egyéb termékek mellett, vagy azért mert nem akarják, hogy a gyermekük jelenlegi kezelése megszakadjon, vagy azért mert inkább egy teljesebb növényi kivonatot akarnak alkalmazni az egyetlen összetevőjű Epidiolex helyett.
“A gyermekem stabil. Én nem nyúlok hozzá,” mondta Allison Ray Benavides, akinek 6 éves fia Robby olyan kannabisz olajat használ amihez egy kevés THC-t adnak.
Robbynak 15-25 rohama volt egy nap, még akkor is amikor a felírt epilepszia ellenes gyógyszert, a Depakote-t szedte, és volt, hogy sisakot viselt minden nap, hogy megvédje a fejét az esésektől.
Mióta két évvel ezelőtt elkezdte a kannabisz olajat összesen csak öt rohama volt.
“Nincs szükségem egy kettős-vak, placebo-kontrollos vizsgálatra, hogy tudjam mi történik,” mondta Ms. Ray Benavides, egyúttal azonban üdvözölte a Epidiolex vizsgálati eredményeket.
Az elemzők azt várják, hogy az Epidiolex költsége 2500-5000 USD lesz havonta, ami drágább, mint az orvsosi kannabisz termékek, amelyek ára körülbelül 100-1000 USD havonta. Azonban lehet, hogy az Epidiolex-et fedezni fogja a biztosítás, ellentétben a többi termékkel.
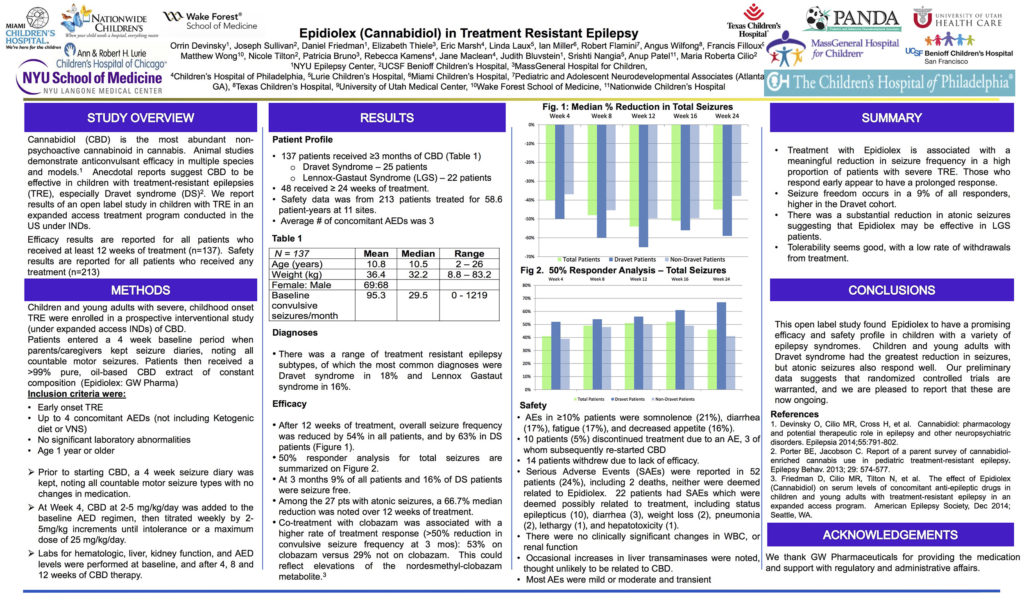
Az Epidiolex (Kannabidiol) Hatásossága és Biztonságossága Gyermekekben és Fiatal Felnőttekben Terápiarezisztens Epilepsziával: Frissítés a Kiterjesztett Hozzáférésű Programból
MAGYARÁZAT:
A kannabidiolt (CBD) a leggyakoribb nem-pszichotróp kannabinoid a kannabisz növényben. Állatkísérletek bizonyítjákgörcsoldó hatékonyságát különböző fajokban és modellekben. Anekdotikus beszámolók alapján hatásos terápiarezisztens epilepsziás (TRE) gyeremekeknél, beleértve a Dravet szindrómát (DS) és a Lennox-Gastaut szindrómát (LGS). Jelentést teszünk a jelenlegi eredményekről a kiterjesztett hozzáférésű kezelési programban.
MÓDSZER:
TRE-vel rendelkező gyermekek és fiatal felnőttek vettek be egy prospektív megfigyeléses vizsgálatba, egy kiterjesztett hozzáférésű különleges kezelési CBD programban. A 4 hetes kiindulási időben a szülők/gondozók roham naplót vezettek minden megszámlálható motor roham típusról. A betegek egy erősen standardizált növényi eredetű, tisztított CBD gyógyszert kaptak. (Epidiolex®: GW Pharma), fokozatosan növekvő adagot kaptak 2-5 mg/kg/nap-tól amíg intolerancia jelentkezett, vagy nem érték el a maximális 25 mg/kg/nap adagot. A betegek rendszeres időközönként viziten vettek részt 2-4 hetente a 12 hetes terápia kezdeti időszaka alatt. Vér, máj és vese működést teszteltünk és AED (epilepszia ellenes gyógyszerek) szint mérést végeztünk a kiinduláskor, majd 4, 8 és 12 héttel a CBD terápia megkezdése után.
EREDMÉNYEK:
261 beteg kapott legalább 3 hónapos kezelést és adatok biztosított az utolsó csoport adatgyűjtéskor (136 (52%) férfi; átlagéletkor 11,8 év, tartomány 4 hónap-41 év; átlagos súly 38 kg; tartomány 6,4-127). A leggyakoribb diagnosis a DS (44; 17%) és a LGS (40; 15%) voltak. Az átlagos egyidejű AED 3,0 volt. A 3 hónapos terápia után a medián teljes rohamgyakoriság csökkenés 45,1% az összes betegnél, és 62,7% a DS betegeknél. A LGS betegeknél a medián csökkenése az atóniás rohamokban a kiindulási értékhez képest 71,1%. Az összes beteg 47%-ánál ≥50%-kal csökkentek a rohamok. Rohammentesség 3 hónap után a betegek 9%-ánál és a DS betegek 13%-ánal alakult ki. A klobazám (clobazam) együttes adása mellett magasabb volt a terápiás válasz (≥50% rohamcsökkenés csökkentés): 57% v. 39%; ez tükrözheti a dezmetil klobozám metabolit emelkedését. Biztonsági adatok 313 betegtől, amik 180 beteg-évet jelentenek 16 helyszínen voltak elérhetők. Nemkívánatos események a betegek ≥10%-ánál aluszékonyság (23%), hasmenés (23%), kimerültség (17%), csökkent étvágy (17%), rohamok (17%) és hányás (10%). 14 betegnél (4%) volt olyan nemkívánatos esemény, ami a CBD kezelés felfüggesztéséhez vezetett. 36 beteg (12%) abbahagyta a kezelést, elsősorban a hatásosság hiánya miatt. Súlyos mellékhatást 106 beteg (34%) jelentett, ezen belül 7 haláleset, de egyik sem volt a kezeléssel kapcsolatos. 16 beteg (5%) jelentett súlyos mellékhatásokat, amelyek összefüggésben voltak a kezeléssel, ezek között volt a megváltozott májenzimek (4 pont, mindegyikük szedett valproátot és klobazámot is), status epilepticus/görcsroham (4), hasmenés (4), testsúlycsökkenés (3) , trombocitopénia (1), és mások.
KÖVETKEZTETÉSEK:
Ezek egy ellenőrizetlen tanulmányból származó eredmények támogatják az állatkísérleteket és a korábbi jelentéseket, amit azt mutatják, hogy a CBD ígéretes kezelés lehet TRE esetében, és általában jól tolerálható akár 25 mg/kg/nap dózisban is. Az Epidiolex®-et most randomizált, kontrollált DS és LGS kísérletekben vizsgálják.
Ez a cikk a Magyar Orvosi Kannabisz Egyesület önkénteseinek munkájában készült. Az Egyesület egyik hivatalos facebook csoportja, ami kizárólag CBD olaj használatával, tapasztalatok megosztásával foglalkozik: https://www.facebook.com/groups/482424458549382/. Mielőtt bárki CBD terméket vásárolna, kérjük csatlakozzon, hogy ne legyen átverés áldozata. Az egyesület munkáját, mivel nonprofit szervezetről van szó, ha csak pár 100 ft-tal is ezen az oldalon lehet támogatni. Kérünk mindenkit, támogassa munkánkat, hogy segíthessünk!
https://orvosikannabisz.com/tamogatas/
Forrás:
https://www.aesnet.org/meetings_events/annual_meeting_abstracts/view/2414222
http://www.nytimes.com/2016/03/15/business/marijuana-based-drug-found-to-reduce-epileptic-seizures.html?emc=eta1&_r=3
https://globenewswire.com/news-release/2016/03/14/819375/0/en/GW-Pharmaceuticals-Announces-Positive-Phase-3-Pivotal-Study-Results-for-Epidiolex-cannabidiol.html
http://www.gwpharm.com/GW%20Pharmaceuticals%20Announces%20Positive%20Phase%203%20Pivotal%20Study%20Results%20for%20Epidiolex%20cannabidiol.aspx
http://www.gwpharm.com/GW%20Pharmaceuticals%20Announces%20New%20Physician%20Reports%20of%20Epidiolex%20Treatment%20Effect%20in%20Children%20and%20Young%20Adults%20with%20Treatment-Resistant.aspx
http://www.gwpharm.com/uploads/cbdposteraan-r_08apr2015.pdf
http://www.firstwordpharma.com/node/1344542?tsid=1#axzz3xJ3MFelc
https://www.aesnet.org/meetings_events/annual_meeting_abstracts/view/1868391
https://www.aesnet.org/meetings_events/annual_meeting_abstracts/view/1868751