SAGE Open Medical Case Reports
A kannabidiol használatának feltűnő hatása tüdőrákban, esettanulmány és irodalmi áttekintés:
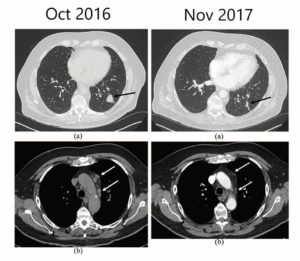
Az új gyógyszerek ellenére a tüdőrák nagyon rossz előrejelzéssel jár. Míg a célzott terápiák javítják az eredményeket, nem gyakori, hogy sok betegnek csak részleges válaszreakciója van, és a nyomonkövetés során visszaesés következik be. Tehát még mindig szükség van új gyógyszerekre vagy más, nem malignus betegségek kezelésére használt gyógyszerek újraértékelésére. Miközben ezek a kutatások mind in vitro, mind in vivo folyamatban vannak, fontos, hogy figyeljünk azokra a betegekre, akiknél a betegség reagál a klinikai gyakorlatban nem standardnak minősülő kezelésekre. Itt egy tüdő adenokarcinómában szenvedő betegről számolunk be, aki miután visszautasította kemoterápiát és a sugárterápiát, tumorválaszt ért el kannabidiol használatával, ami a Cannabis sativa, nem-pszichotróp vegyülete. Korábbi kutatások kimutatták, hogy a kannabidiol antioplasztikus tulajdonságokkal rendelkezik és fokozhatja a rák elleni immunválaszt. Az itt bemutatott adatok azt mutatják, hogy a kannabidiol a tüdőrákos betegeknél feltűnő reakciót eredményezett. TOVÁBB
Read more